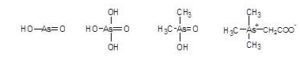
三塩化ヒ素(Arsenic trichloride)は、AsCl3という化学式を持つ無機化合物である。毒性を持つ油状の物質で無色であるが、不純物を含むものは黄色を呈する。有機ヒ素化合物を製造する際の中間体となる。
構造
三塩化ヒ素は、C3v対称性を持つピラミッド状の分子である。As-Cl結合は2.161Åの長さで、Cl-As-Clの角は98°25'±30である。三塩化ヒ素は、ν1(A1) 416、ν2(A1) 192、ν3 393、ν4(E) 152 cm-1の4つの通常振動モードを持つ。三塩化ヒ素はほぼ共有結合であり、そのため融点は低い。
合成
三塩化ヒ素は、三酸化二ヒ素を塩化水素で処理し、その後蒸留することによって製造される。
また、ヒ素を80〜85℃で塩素化することによっても得られるが、この方法には、ヒ素元素が必要である。
酸化ヒ素と一塩化硫黄の反応によっても得られる。この方法は単純な器具しか必要とせず、また効率よく進む。
反応
水による加水分解で、亜ヒ酸と塩酸になる。
三塩化ヒ素は三塩化リンよりも感湿性が弱いが、それでも湿気を含んだ空気中では気化する。
三酸化二ヒ素で処理することで、無機ポリマーのAsOClを形成する。塩素源の下では、三塩化ヒ素は [AsCl4]-を含む塩を形成する。臭化カリウムやヨウ化カリウムと反応させると、それぞれ三臭化ヒ素や三ヨウ化ヒ素が得られる。有機ヒ素化合物の合成に有益で、三塩化ヒ素からトリフェニルアルシンが合成される。
安全性
ヒ素化合物は非常に毒性が高いが、三塩化ヒ素はその揮発性や溶解性のために、特に毒性が高い。
出典